在细胞的精细调控网络中,表皮生长因子受体(EGFR)家族如同一群掌控生长与分化的“指挥官”,通过精准获取外部信号来调节细胞的增殖、凋亡与迁移。然而,当这些“指挥官”因基因突变、扩增等原因失控后,它们便可能转变为癌细胞狂野生长的“帮凶”。作为癌症治疗领域的核心靶点,EGFR家族的研究不仅揭示了肿瘤发生的重要机制,还推动了从单克隆抗体到小分子靶向药物的革命性进步。
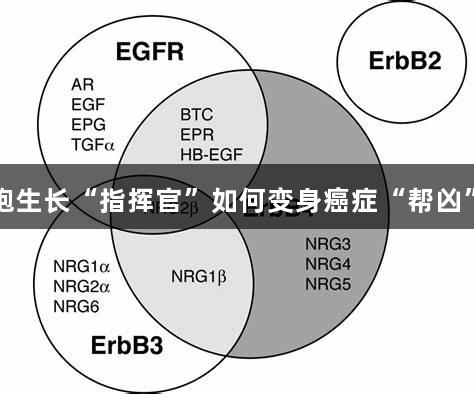
EGFR家族由EGFR(HER1)、HER2、HER3和HER4四个成员构成,作为跨膜酪氨酸激酶受体,它们通过“胞外结构域识别信号-跨膜结构域传递信号-胞内结构域激活通路”的三级联动,建立起细胞生长的调控中心。在正常组织中,EGFR家族是发育与稳态的守护者,但在肿瘤中由于多重机制的影响,EGFR通路失控为癌细胞提供三大“生存武器”:加速G1/S期转换的增殖引擎、抑制线粒体凋亡通路的抗凋亡护盾,以及促进基质降解与血管新生的转移助力。这些变化共同构成肿瘤恶性演进的分子基础。
针对EGFR家族的靶向药物以“胞外阻断”与“胞内抑制”双策略展开,但却面临耐药性带来的严峻挑战:EGFR家族的研究历史,恰是从基础分子机制到临床转化的“精准医学进化史”。尽管耐药性依然是当前的发展瓶颈,其复杂的调控网络也为新药研发提供了丰厚的靶点——从HER3抗体MM-121到双特异性抗体MM-151,从表观调控到肿瘤微环境干预,多学科交叉正催生出更多创新疗法。
未来,伴随着液体活检和AI辅助药物设计的普及,EGFR家族相关肿瘤治疗将开启“分型更精准、耐药可预测、方案个性化”的新时代,使得“精准打击癌细胞,保留正常细胞”的医疗愿景逐渐成为现实。在这场持续数十年的“抗癌战争”中,EGFR家族既是难以对付的敌人,也是关键的突破口。随着研究的深入,人类终将破解这些“信号指挥官”的失控密码,为癌症治疗开辟出更广阔的精准化之路。
尊龙凯时致力于为全球生命科学行业提供高质量的抗体、蛋白、试剂盒等产品及研发服务。依托多个开发平台,包括重组兔单抗、重组鼠单抗、快速鼠单抗以及重组蛋白开发平台(Ecoli, CHO, HEK293, Insect Cells),已通过欧盟98/79/EC认证、ISO9001认证和ISO13485认证。


